Autores: María José Goncalves, Daniela Maspero / Unidad de Química y Ambiente. Centro de Tecnología de Materiales (CTM). FIIIDT.
1.- Introducción
En el caso de aguas residuales es de gran importancia conocer los contaminantes presentes para actuar inmediatamente en el caso de un impacto negativo en el medio y prevenir contaminación de lagos, ríos, acuíferos, lagunas y mar, así como impactos en la flora y fauna.
La tecnología aplicada al tratamiento de aguas residuales ha crecido con el tiempo y por lo tanto ha aumentado el interés en realizar la caracterización fisicoquímica y microbiológica del agua. Con este análisis se podrá diseñar y operar adecuadamente las plantas de tratamiento, esto con la finalidad de reutilización y reciclaje de este recurso imprescindible para la vida.
Cuando se habla de aguas residuales podemos mencionar tres características principales:
1.- Elevada carga orgánica.
2.- Presencia de componentes tóxicos para los microorganismos.
3.- Presencia de sustancias no biodegradables.
Las aguas residuales se han clasificado en tres tipos según su procedencia:
1.- Agua residual doméstica, son las provenientes de zonas de vivienda y de servicios generadas por el metabolismo humano y las actividades domésticas.
2.- Agua residual industrial son todas aquellas vertidas por empresas comerciales e industriales.
3.- Agua residual urbana en este grupo entran mezclas de aguas domésticas, industriales y aguas de escorrentías pluvial. Todas estas en teoría se acumulan en un colector y son llevadas a una planta de tratamiento.
La selección de los parámetros a ser analizados viene determinada en función de la procedencia de las aguas residuales, su tratamiento y el destino final de las mismas. En nuestro país los laboratorios autorizados por el Ministerio del Poder Popular para el Ecosocialismo (MINEC), entre ellos los laboratorios de Química y Ambiente de la FIIIDT (N° LDP 01-044), se rigen por lo reglamentado en la Gaceta Oficial No 5021 Extraordinario del 18 de noviembre de 1995. También es necesario señalar quelas técnicas de muestreo, preservación de muestras y determinación de los parámetros fisicoquímicos y biológicos, se llevan a cabo, en su mayor parte, bajo las normas del “Standard Methods for the Examination of Water and Wastewater, 21th Edition, 2005”.
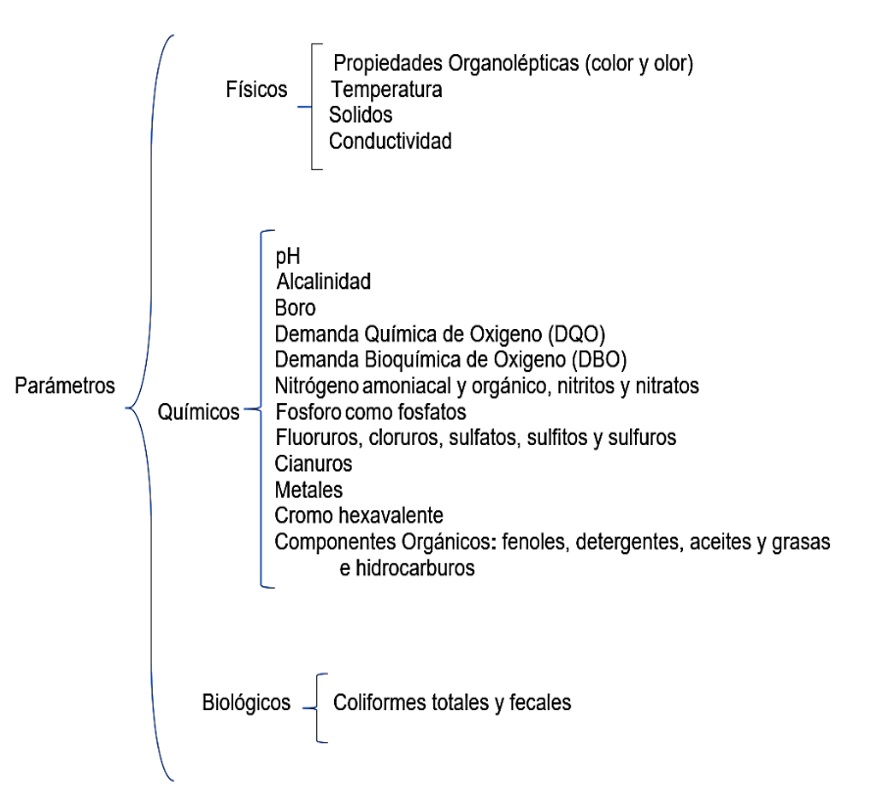
A continuación, se presenta un esquema de los parámetros que se determinan en la institución para caracterizar las muestras de agua residual.
2.- Muestreo
En el artículo anterior sobre caracterización de agua potable [5], se han descrito las técnicas de captación de muestra, tipos de muestra que se toman (puntual, compuesta o integrada), preservación de acuerdo al parámetro a determinar y las medidas de seguridad a seguir durante las operaciones de muestreo de agua. En dicho artículo también se han dado las condiciones de preservación para los siguientes parámetros: color, cloruros, cianuros, fluoruros, nitratos, nitritos, sulfatos, fenoles, metales, oxígeno disuelto y coliformes; que junto con los que se presentan en la tabla 1 forman parte importante en la evaluación de las muestras de agua residual. Las mediciones de pH, temperatura y conductividad se realizan directamente en campo.
Tabla 1. Preservación y almacenamiento de muestras de agua de acuerdo los diferentes parámetros [6]
|
Parámetro |
Tipo de envase |
Tamaño mínimo de muestra, en ml |
Tipo de muestra |
Preservación |
Tiempo Máximo de almacenamiento |
|
|
Aceites y grasa, e
Hidrocarburos |
Recipiente de vidrio con boca ancha de 1 L |
1000 |
Puntual |
Adición de H2SO4 o HCl a pH< 2 y refrigeración a T≤ 6°C |
28 días
|
|
|
Alcalinidad
|
P, V o T |
100
|
Puntual |
Refrigeración a T ≤ 6°C y analizar inmediatamente |
24 horas |
|
|
Boro |
P, T o Cuarzo |
1000 |
Puntual y compuesta |
Añadir HNO3 a pH< 2 y luego refrigerar a T ≤ 6°C |
28 días |
|
|
Detergentes |
P, V o T |
250 |
Puntual y compuesta |
Refrigeración a T ≤ 6°C |
48 horas |
|
|
DBO |
P, V o T |
1000 |
Puntual y compuesta |
Refrigeración a T ≤ 6°C |
6 horas |
|
|
DQO |
P, V o T |
100 |
Puntual y compuesta |
Analizar tan pronto como sea posible o adicionar H2SO4 a pH< 2 y refrigeración a T ≤ 6°C |
7 días en caso de muestra preservada |
|
|
Fosforo Total |
V(A) |
100 |
Puntual y compuesta |
Adición de H2SO4 a pH< 2 y refrigerar a T ≤ 6°C |
28 días |
|
|
Cromo hexavalente |
P(A), V(A) o T(A) |
250 |
Puntual |
Ajustar el pH de la muestra entre 9,3 y 9,7 con pequeñas adiciones de buffer de (NH4)2SO4 y NaOH 5N y refrigerar a T ≤ 6°C hasta el momento del análisis. No dluir la muestra más del 10%. |
28 días |
|
|
Nitrógeno Amoniacal |
P, V o T |
500 |
Puntual y compuesta |
Analizar tan pronto como sea posible o adicionar H2SO4 a pH< 2 y refrigeración a T ≤ 6°C |
7 días en caso de muestra preservada |
|
|
Nitrógeno Orgánico |
P, V o T |
500 |
Puntual y compuesta |
Adicionar H2SO4 a pH< 2 y refrigerar a T ≤ 6°C |
7 días |
|
|
Solidos |
P o V |
200 |
Puntual y compuesta |
Refrigeración a T ≤ 6°C |
7 días |
|
|
Sulfitos |
P o V |
500 (llenar el recipiente completamente para excluir el aire) |
Puntual y compuesta |
Adición de 1 ml de EDTA 2,5% en peso /100 ml de muestra. Refrigerar a T ≤ 6°C |
2 días |
|
|
Sulfuros |
P, V o T |
100 (llenar el recipiente completamente para excluir el aire) |
Puntual y compuesta |
Añadir 4 gotas de acetato de cinc 2N/100 ml de muestra. Adicionar NaOH a pH>9 y refrigerar a T ≤ 6°C |
28 días |
|
Abreviaturas
P: plástico (polietileno o equivalente); V:vidrio;T:teflón
P(A), V(A), T(A): envases de plástico, vidrio y teflón, respectivamente, lavados con solución de ácido
Nítrico (HNO3) 50%volumen de reactivo como parte de la limpieza de estos envases.
DBO:Demanda Bioquímica de Oxigeno
DQO: Demanda Química de Oxigeno
H2SO4: ácido sulfúrico
HCl: ácido clorhídrico
NaOH: hidróxido de sodio
Na2S2O3: tiosulfato de sodio
(NH4)2SO4: sulfato de amonio
3.- Parámetros
En la tabla 2 se presentan las técnicas analíticas utilizadas para la cuantificación de los parámetros [6] nombrados en la tabla 1 y en las secciones siguientes se definen cada uno de estos.
3.1- Parámetros Físicos
3.1.1- Sólidos
Se definen como todos aquellos elementos o compuestos presentes en el agua que no son aguas ni gases. Se pueden clasificar en tres grupos: totales, disueltos y suspendidos. La medida de los sólidos totales es un índice de la cantidad de sustancias disueltas en el agua y proporciona una indicación general de su calidad química. Los sólidos disueltos están definidos analíticamente como residuo filtrable y corresponden a carbonatos, bicarbonatos, cloruros, sulfatos, fosfatos, calcio, magnesio, sodio, etc. Por otro lado, se define como sólidos suspendidos aquella materia orgánica e inorgánica particulada existente en el agua (aceites, grasas, arcillas, arenas, fango, etc.) [7].
3.2- Parámetros Químicos
3.2.1- Aceites y Grasas
Se incluyen aquellas que están en estado libre ya sean de origen animal, vegetal o mineral, destacando entre estos últimos por su especial importancia los derivados del petróleo. La mayoría son insolubles en agua, pero pueden existir en forma emulsionada o saponificada.
3.2.2- Hidrocarburos
Serie de compuestos que presentan en su estructura átomos de carbono y de hidrógeno. Se pueden diferenciar dos grupos de hidrocarburos, los derivados del petróleo y los aromáticos policíclicos.
3.2.3- Alcalinidad
La alcalinidad de una muestra de agua es su capacidad para neutralizar compuestos ácidos. Aunque son muchos los materiales que pueden contribuir a la alcalinidad, de aguas naturales o tratadas; esta es primariamente una función de su contenido de carbonatos, bicarbonatos e hidróxidos.
3.2.4- Boro
El boro es un elemento natural que se encuentra con más frecuencia como ácido bórico y boratos y está asociado a la salinidad en aguas. Se encuentra en el agua de mar y en descargas de plantas de tratamiento de aguas residuales, en donde se utilizan jabones, detergentes y fertilizantes. A niveles mayores de 2 mg/L la mayoría de los cultivos agrícolas presentan problemas de toxicidad [8].
3.2.5- Demanda Bioquímica de Oxigeno
Es la cantidad de oxígeno que necesitan los microorganismos para degradar la materia orgánica presente en el agua durante 5 días a 20°C. Se cuantifica mediante la medición electrométrica de oxígeno disuelto antes y después del procesamiento de la muestra. A este parámetro se le denomina DBO5.
3.2.6- Demanda Química de Oxigeno (DQO)
Este parámetro mide la porción de materia orgánica biodegradable o no de una muestra que es susceptible a la oxidación por un oxidante fuerte (K2Cr2O7).
3.2.6- Detergentes
Son productos formados por agentes surfactantes y compuestos minerales (carbonatos, fosfatos, polifosfatos, etc.). De todos los productos los más característicos son los surfactantes.
3.2.7- Nitrógeno
El nitrógeno es esencial para el crecimiento de microorganismos y plantas. Este elemento se encuentra presente en el agua residual en forma orgánica (urea y proteínas), como nitrato de amonio en fertilizantes agrícolas y como nitritos, los cuales son considerados indicadores indirectos de contaminación fecal.
3.2.8- Fosforo
Su contenido proviene de tres tipos de compuestos a saber inorgánicos, orgánicos y en tejidos vivos. En la actualidad la mayor fuente de aporte de fósforo proviene de los detergentes.
3.2.9- Sulfitos
Los sulfitos son especialmente utilizados como conservantes para alimentos debido a su efecto inhibitorio sobre el crecimiento microbiano, pero a altas concentraciones hace difícil el tratamiento biológico de las aguas residuales que lo contienen [9].
3.2.10- Sulfuros
Los sulfuros en aguas residuales provienen de la descomposición de la materia orgánica y de la reducción bacteriana de sulfatos y sulfitos. El sulfuro de hidrogeno que se desprende es un gas inflamable, incoloro, muy tóxico y con olor desagradable. Los niveles máximos permitidos de sulfuro en aguas van de 0.5 a 2 mg/L [10] según hacia donde sea descargada (ríos, lagunas, mar o redes cloacales) el agua residual.
3.2.11- Fenoles
Los compuestos fenólicos pueden afectar a las especies por toxicidad directa y por disminución de la cantidad de oxígeno disponible debido a su elevada demanda de este gas.
3.2.12- Cromo Hexavalente
El cromo se encuentra en dos estados de oxidación: Cr (III) o Cr (VI), de los cuales el más toxico es este último. Los derivados del cromo hexavalente (cromatos y dicromatos), se utilizan en metalurgia, curtido de cueros y en fabricación de pinturas; contaminando de esta forma los cuerpos de agua y suelos; y son cancerígenos para el ser humano [11].
Tabla 2. Técnicas analíticas utilizadas para la determinación de los parámetros para caracterización de agua residual
| PARÁMETRO | TÉCNICA ANALÍTICA | N° DE MÉTODO |
| Solidos (totales, suspendidos y disueltos) | Gravimetría | 2540 |
| Aceites y Grasas, Hidrocarburos | Extracción y gravimetría | 5520B y 5520F |
| Alcalinidad | Volumetría | 2320 |
| Boro | Espectrofotometría UV-visible | 4500-B C |
| Demanda Química de Oxigeno (DQO) | Reflujo cerrado + Espectrofotometría UV-visible | 5220-COD D |
| Demanda Bioquímica de Oxigeno (DBO) | Proceso biológico y medición electrométrica de oxígeno disuelto | 5210-BOD B |
| Nitrógeno Amoniacal | Destilación + Volumetría | 4500-NH3 B y C |
| Nitrógeno Orgánico | Método Macro- Kjeldahl | 4500-Norg B |
| Fosforo | Espectrofotometría UV-visible | 4500-P C o 4500-P E |
| Fosforo | Cromatografía Iónica | Bajo condiciones específicas del equipo |
| Sulfitos | Volumetría | 4500- SO3-2 B |
| Sulfuros | Volumetría | 4500- S-2 F |
| Sulfuros | Espectrofotometría UV-visible | 4500- S-2 D |
| Fenoles | Extracción + Espectrofotometría UV-visible | 5530 |
| Detergentes | Extracción + Espectrofotometría UV-visible | 5540 C |
| Cromo Hexavalente | Espectrofotometría UV-visible | 3500-Cr B |
Nota: los métodos que están numerados se realizan en base a la referencia del Standard Methods for the Examination of Water & Wastewater, 21st Edition, 2005 [6]
BIBLIOGRAFIA
2.- https://www.contruyenpais.com
4.- cidta.usal.es > Pasar>Aguas-Residuales-composicion.pdf
5.- María José Goncalves, Daniela Maspero Laboratorio de Química y Ambiente. Caracterización de Muestras de Agua Potable Nota Técnica. Unidad de Química y Ambiente. Centro de Tecnología de Materiales (CTM). FIIIDT.2020: http://www.fii.gob.ve/laboratorio-de-quimica-y-ambiente-caracterizacion-de- muestras-de-agua-potable/
6.- Standard Methods for the Examination of Water and Wastewater, 21th Edition, 2005
8.- https://www.lenntech.es/procesos/mar/post-tratamiento/general/-boron- removal.htm
9.- Lizeth Cristina Rodríguez Núñez. 2018-2019. Eliminación de Altas Concentraciones de Sulfitos de Aguas Residuales de la Industria Agroalimentaria mediante un Reactor Biológico Secuencial. Universidad Politécnica de Valencia.
10.- Gaceta Oficial N° 5.021 Extraordinario del 18 de diciembre de 1995. Normas para la Clasificación y el Control de la Calidad de los Cuerpos de Agua y Vertidos o Efluentes Líquidos. Capitulo III.
11.- Carlos Alberto Severiche Sierra y Humberto González García. Verificación Analítica Para las Determinaciones de Cromo Hexavalente en Aguas por Espectrofotometría Ing. USBMed, Vol. 4, No. 1, enero-junio 2013
Contactos: mariajog1903@gmail.com, maspero.daniela@gmail.com
